2016-2022 All Rights Reserved.平安财经网.复制必究 联系QQ 备案号:
本站除标明“本站原创”外所有信息均转载自互联网 版权归原作者所有。
邮箱:toplearningteam#gmail.com (请将#换成@)
使用光遗传技术,使用小于一粒米的微型线圈可以改善针对神经元的可植入光学装置。科学家可以利用这种方法传播光脉冲,在转基因神经元中打开或关闭蛋白质表达。到目前为止,神经科学家已经使用笨重的电缆和电池来控制和收集来自这些实验装置的数据。在最近的一项研究中,Wasif Khan和美国电子与计算机工程与生理学跨学科的一组研究人员开发了一种完全无线的原型来取代庞大的硬件。
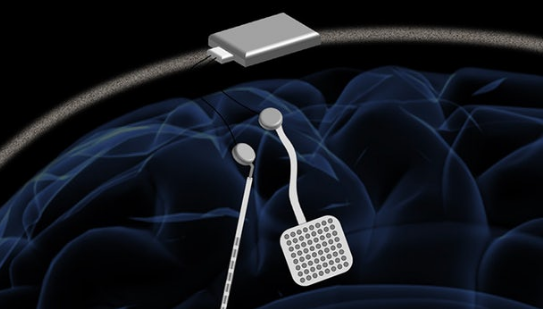
为此,该团队将微型发光二极管(LED)与两个毫米级线圈相结合,创建了一个感应充电系统,在实验性啮齿动物(大鼠)模型中以生物安全频率提供瞬时功率。的无线设置中刺激神经元视觉皮层,同时保持温度升高低于1 0 C作为用于生物医学植入物的一个关键安全性阈值。结果现已发布在Microsystems和Nanoengineering上。
汗等人。他介绍了一种单通道神经刺激器,它包含一个反射器耦合的微型发光二极管(μLED)和一个集成的毫米级无线接收器(R X)线圈。实验装置允许自由浮动,无电池,不受限制的光遗传学神经调节。他们在系统中使用双线圈感应链路,以低工作频率(<100 MHz)提供瞬时功率,以实现连续光学刺激。
该过程对电磁辐射造成最小的侵入性和组织暴露。当他们将微型反射器耦合到μLED时,与裸μLED相比,光学反射器显示出显着增强的光强度。科学家控制了植入物生物相容性设置的操作温度,并在大鼠体内进行了实验,随后进行了组织学研究,以验证无线光学刺激在动物模型的初级视觉皮层中的功效。他们使用c-Fos生物标记物可视化该过程,该标记物在免疫染色时显示为绿色,作为光诱发神经元活动的报告物。
神经科学中的发现和发明最近由于神经生物学系统中半导体植入物的进步而迅速发展,用于成功的临床翻译。例如,科学家可以在新的医学方法中使用植入式“电疗法”,以在治疗干预期间靶向中枢和外周神经系统。因此,光遗传学正在神经科学中寻找新的应用,将光传递给感兴趣的神经组织,同时使用靶向控制工具从细胞中收集读数。
将微型光源,记录电极,传感器和其他组件植入大脑的指定区域的能力再次激发了对长期诊断和治疗的乐观。利用这些发展,科学家们可以研究将初级感觉信息传递到大脑的特定区域,包括嗅觉,视觉和听觉区域的深度。他们还可以使用该技术来了解通过活动模式驱动或抑制饥饿,口渴,能量平衡和呼吸等基本生物活动的细胞。
表征结果和操作原型的图像。(a,b)蚀刻的Si腔的SEM图像。(c,d)分别对腔体进行后涂层和先前的Al涂层。(e,f)用于腔表面粗糙度的定量分析的AFM图像(以μm为单位的x轴单位,以nm为单位的y轴)。(g)制造的单通道光学神经刺激器。h Rx线圈耦合单通道光学神经刺激器。(i,j)光学刺激器由Tx线圈无线供电。图片来源:Microsystems&Nanoengineering,doi:10.1038 / s41378-019-0061-6
光遗传学必须针对神经群体,而不改变动物模型的自然行为,以便在医学中准确应用。该领域研究人员的开创性工作已经开发出几种具有中场射频(RF)和远场功率传输的优化神经刺激器。然而,科学家尚未报道完全可植入和小型化的高压(HV)刺激器,它可以对感兴趣的参数进行精确的刺激控制。因此,理想的无线光学植入物必须:
是毫米级(mm)的缩影,以防止侵入性手术感染,炎症和手术后创伤。
允许高效的功率传输和与深部区域目标神经元的长距离通信,目的是人类应用。
设计这种植入物的一个重大挑战是光学激活光遗传学视蛋白所需的能量,其通常包括几mW,尽管大于常规电刺激或数据通信的值。为了解决这一挑战,Khan及其同事提出了一种完全可植入的迷你无线光学刺激器,可为μLED操作提供足够的功率 - 而不会超过工作温度。在所提出的系统中,它们包括螺线管发射器(T X)线圈和接收器(R X)单元。
在提出的原型的概念验证中,Khan等人。使用270μm×220μm表面积的蓝色μLED(465nm波长)来光学激发表达通道视紫红质的神经元。为了在动物模型中验证设备的功能,科学家将Tx线圈放置在大脑外并将其电感耦合到Rx线圈,Rx线圈集成到放置在开颅腔内的μLED神经刺激器。科学家们使用自由漂浮法在硬脑膜顶部的开颅腔内进行硬膜外光学神经调节。
TOP:横截面平面感应耦合的仿真模型。平面3指的是Tx线圈的底平面(z轴位移,z = 0),平面1,2,4分别指z = 2.5mm,z = 1mm和z = -1mm。(a)HFSS中的模拟模型。(b)平面1,(c)平面2,(d)平面3和(e)平面的磁通分布4.在平面2处由Rx线圈感应磁通量,而Rx位于f Tx中心并且g Tx周边。色彩图图例中提供的通量分布单位。底部:光学和热学特性。(a)透过具有耦合反射器的组织切片的光穿透(n = 5),(b)与裸μ-LED相比,反射器耦合刺激器的强度改善,和(c)通过500μm皮质刺激的装置的温度变化组织切片(n = 3)。
科学家使用扫描电子显微镜测试了原型的表面形态,观察了各向同性硅蚀刻和表面铝涂层后的腔阵列。然后,他们使用原子力显微镜测试表面粗糙度,以检测产生可忽略的光散射的表面,以获得最佳增强的光强度,并通过感应供电在台式设置上激活神经刺激器。科学家们还掺入聚对二甲苯-C工程师由于材料的固有的生物相容性的构建体中,虽然他们观察到潜在的裂纹如前如在工程过程高的温度的结果。
汗等人。使用有限元法(FEM)和高频结构刺激器(HFSS)软件模拟Rx和Tx线圈之间的感应链路的电磁特性; 显示模拟Tx线圈与工作中设计的线圈之间的相似性。科学家研究了光学特性,结果表明,与波导或穿透探针相比,神经刺激器可以更少侵入性地进入深部脑细胞。虽然数据显示反射器耦合刺激器的优异光学性能,但是随着较厚的组织切片,强度显着降低。与裸露的刺激器相比,目前的工作中反射器耦合刺激器的强度明显更高有效的深部脑刺激,无深部脑组织侵犯。汗等人。类似地测试和优化了神经刺激器原型的热特性,电磁特性和功率传递效率。为了在动物模型中进行转化研究,科学家们提出将谐振器线圈植入颅骨和皮肤之间,而不需要连接到Tx或Rx线圈。
使用免疫组织学进行系统验证。(a)使用无线驱动的神经刺激器在麻醉的大鼠的V1上进行体内刺激。(b)使用细胞分选定量表示c-Fos表达的细胞。mCherry(c,e)的荧光图像以及对照和刺激皮质的c-Fos(d,f)表达分别从相同转染动物的相同皮质区域获得。(g,h)分别从未转染的动物获得的对照和刺激皮质的c-Fos表达。图片来源:Microsystems&Nanoengineering,doi:10.1038 / s41378-019-0061-6
然后科学家们在转染的大鼠体内进行体内实验(将外源DNA导入细胞),然后实施拟议的外科手术程序。他们按照免疫组织化学分析的实验来验证细胞转染程序和随后的光学刺激程序在大鼠中的功效。在转染期间,它们用病毒溶液在动物模型中诱导通道视紫红质-2的表达,然后将盘绕的刺激物置于动物的初级视觉皮层(V1叶)上用于随后的光学刺激。科学家将盘绕的刺激器与Tx线圈耦合,并使用相同动物的另一个V1叶作为对照样品。
在完成体内实验后,科学家们分析了c-Fos(绿色染料)在受刺激和未受刺激的叶中的表达,以确定神经活动。为此,Khan等人。在工作中使用免疫生物学测定,并观察到由实验神经刺激器的LED刺激诱导的病毒转染的皮质(红色)内升高的c-Fos表达(绿色)。
通过这种方式,Khan等人。设计,制造和表征反射器耦合的无线单通道光学神经刺激器,带有mm尺寸的接收器线圈,用于光遗传学神经调节。与目前工作中的裸μLED相比,反射器耦合刺激器允许更高的性能。科学家研究了双线圈遥测的性能使用分析电路模型,FEM刺激和实验方法进行链接。他们验证了在通过光学刺激观察到的具有上调的细胞活性的大鼠模型中神经刺激器的建议潜力。汗等人。将致力于在未来进行进一步的研究,以使神经生物学应用的装置小型化。
2016-2022 All Rights Reserved.平安财经网.复制必究 联系QQ 备案号:
本站除标明“本站原创”外所有信息均转载自互联网 版权归原作者所有。
邮箱:toplearningteam#gmail.com (请将#换成@)